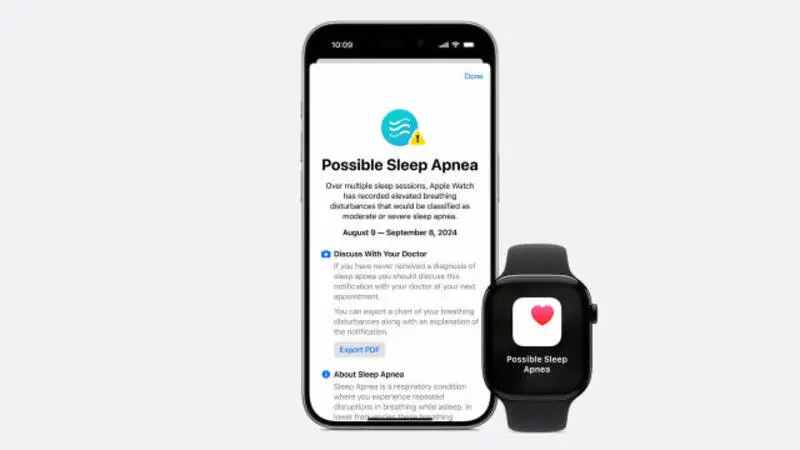
La Administración de Alimentos y Medicamentos de EE.UU. (FDA) aprobó hoy lunes la detección de la apnea del sueño en el Apple Watch Series 9, Series 10 y Watch Ultra 2. La luz verde llega cuatro días antes de la fecha de lanzamiento del Series 10, el 20 de septiembre.
La función, anunciada la semana pasada en el evento del iPhone 16, llegará como parte de la inminente versión watchOS 11. Una vez activada, requiere 10 noches de datos de seguimiento del sueño repartidos en un periodo de 30 días para determinar si un usuario puede padecer la enfermedad. Durante ese tiempo, también ofrece información sobre las alteraciones nocturnas del sueño, utilizando el acelerómetro incorporado.
La FDA clasifica esta función como «dispositivo de venta libre para evaluar el riesgo de apnea del sueño». Apple se apresura a señalar que no se trata de una herramienta de diagnóstico. En su lugar, pedirá a los usuarios que soliciten un diagnóstico formal a un profesional sanitario. Esta afección, que hace que la respiración sea menos profunda o se detenga repetidamente durante la noche, se asocia a una serie de síntomas diferentes. La Clínica Mayo señala que puede causar insomnio, dolores de cabeza, somnolencia diurna y otras afecciones más prolongadas.
Apple no es la primera empresa de electrónica de consumo que ofrece esta función. Withings lleva algún tiempo ofreciendo la detección de la apnea del sueño en sus dispositivos, mientras que Samsung recibió la aprobación de la FDA para su línea Galaxy Watch a principios de este año.
La función llega cuando otra, la detección de oxígeno en sangre, ha sido desactivada en los relojes de Apple en EE.UU. por una disputa de patentes en curso.